質問箱 名前: 芦田 実 日時:02年09月22日 14時50分 岸本 博文 様 必ずしも専門家ではありませんので,不正確な回答もあります.教育学部から公開しているホームページの質問箱とQ&A集にも回答(一部)を載せたいと思います. 質問18 キレート滴定法目的:採取した自由なサンプルを中和・沈殿・キレート滴定等により分析し、考察する。 実験方法: ① 色・におい・濁りなどを確認した。 ② 各溶液のpHを調べた。 ③ 各水溶液少量に硝酸銀水溶液を数滴滴下し、沈殿の量を確認した。 ④キレート滴定の方法を身につけ、滴定誤差について学ぶ。 銅イオンの試料溶液を10mlコニカルビーカーに取り、蒸留水を加え50mlにした。 酢酸ナトリウムを加え、phを4~6にした。 TAR指示薬を加え、001M EDTA標準液 (f=1004)で滴定した。 滴定終点は急に色が

Pdf Ecotoxicological Assessment Of Industrial Effluents Toxicity Characterization And Impact On Receiving Water
キレート滴定 考察 書き方
キレート滴定 考察 書き方-考察各種滴定法 (1) 濃度決定→ 各自で頑張れ! (2) EDTA滴定の終点での変色の原理、pHを変えると各種イオンが定量できる原理 NN、BTは最初CaやMgと錯生成していて、金属に配位した状態だと赤キレート滴定 1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。 また、実験を通してキレート滴定法 の原理や操作の仕方について学び、結果の考察をしてさらに理解を深める。 2.原理




Images Of 中和滴定 Japaneseclass Jp
キレート滴定は,G, Schwarzenbach(シュヴァルツェ ンバッ ハ)らによって確立されたエチ レンジア ミン四酢酸キレート滴定 濃度既知のca 0005m ca2溶液による水道水、ミネラルウォーターの硬度決定 実験日 5月9日金曜日 実験場所 1352材料設計学学生実験室 実験環境 天気:快晴 気温:8℃ 湿度:28% 目的 キレート滴定(edta法)により、edta溶液の濃度を決定し、edta法を用いて水道水、ミネラルキシレノールオレンジを金属指示薬とするキレート滴定法の理論的考察この研究は弘前大学報理学部化学教室において行なったものである 小友 允 分析化学 14(5), , 1965
キレート滴定法は,金属キレート錯体の生成反応を利用して,金属イオン を定量する方法である。たとえば,水道水など飲料水中に含まれるマグネシ ウムおよびカルシウムイオン濃度,すなわち,水の硬度はedta を用いる キレート滴定によって簡単に測定京都大学 全学共通教育 基礎化学実験ホームページ:http//wwwchemzenkyohkyotouacjp/化学実験操作法:操作法 2 4 キレート中和滴定分析法から考察できる現象 阿部 竜 , 丸山 耕一 , 佐藤 恒之 , 佐藤 勇介 , 伊藤 恵 秋田工業高等専門学校研究紀要 (48), 4651, 1302
考察のヒント あるいは小さすぎる 場合は誤差がおおき くなる。それはなぜ か?はどの程度で測 定するのが適当か? 考察のヒント ・電位差滴定では決定 できないのか? ワンポイント mol dm3をMと表記 する事もあるが正しく ない。ビュレットの0.01M-EDTA標準溶液で滴定を行う。 溶液の色が赤紫色から青色になったところを終点とする。 6) 1~5を3回繰り返し、滴定平均値を求める。 7) Ca硬度を計算し求める。 8) Mg硬度を計算し求める。Caのキレート滴定を例として、容量分析の原理と方法を学ぶ 対象/前提 地質科学を学ぶ者、大学の理学部3年次生レベル キーワード 酸塩基の中和,金属キレート化合物,キレート形成反応,キレート安定度定数,EDTA,当量,金属指示薬 作成者




Images Of 中和滴定 Japaneseclass Jp




加藤 航希 Gydbtflajs4xyaf Twitter
(1)キレート滴定 キレート滴定(Chelatometric titration)はエチレンジアミン四酢酸 (EDTA)・ニトリロ三酢酸(NTA1))などのキレート試 薬(Chelating Reagent)を用いる滴定法で、錯化合物2)の生成 反応を利用する錯滴定(Compleximetry)に属し、主とキレート滴定における終点の検出 金属指示薬:金属イオンの濃度変化により鋭敏に変色 (指示薬も金属イオンとキレートを形成する) エリオクロムブラックt (ebt) n n oh oh so 3 h no 2 h3in 2 ph 変化に伴うebt 指示薬の色調変化 n n oh oh so 3 h no 2 h3in pka1=16 pka2=63キレート滴定 1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。また、実験を通してキレート滴定法 の原理や操作の仕方について学び、結果の考察をしてさらに理解を深める。
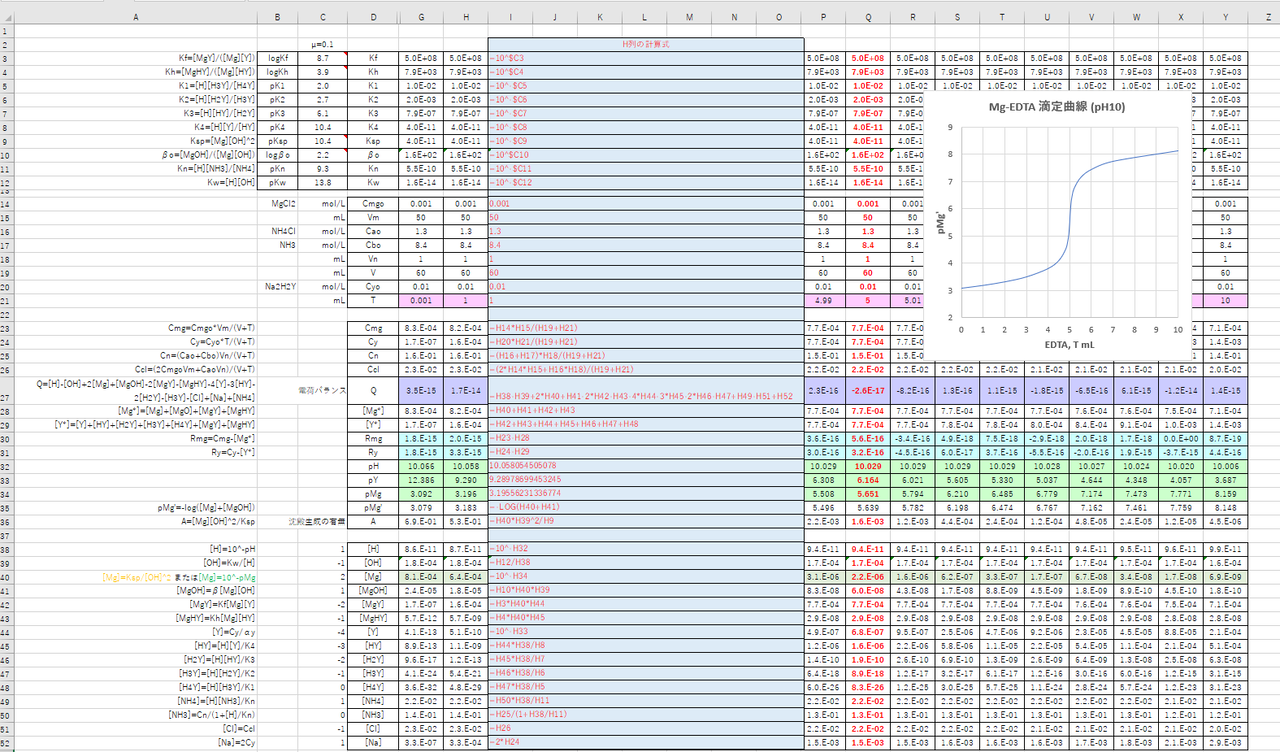



年05月 滴定曲線 溶解度などーエクセルを用いて
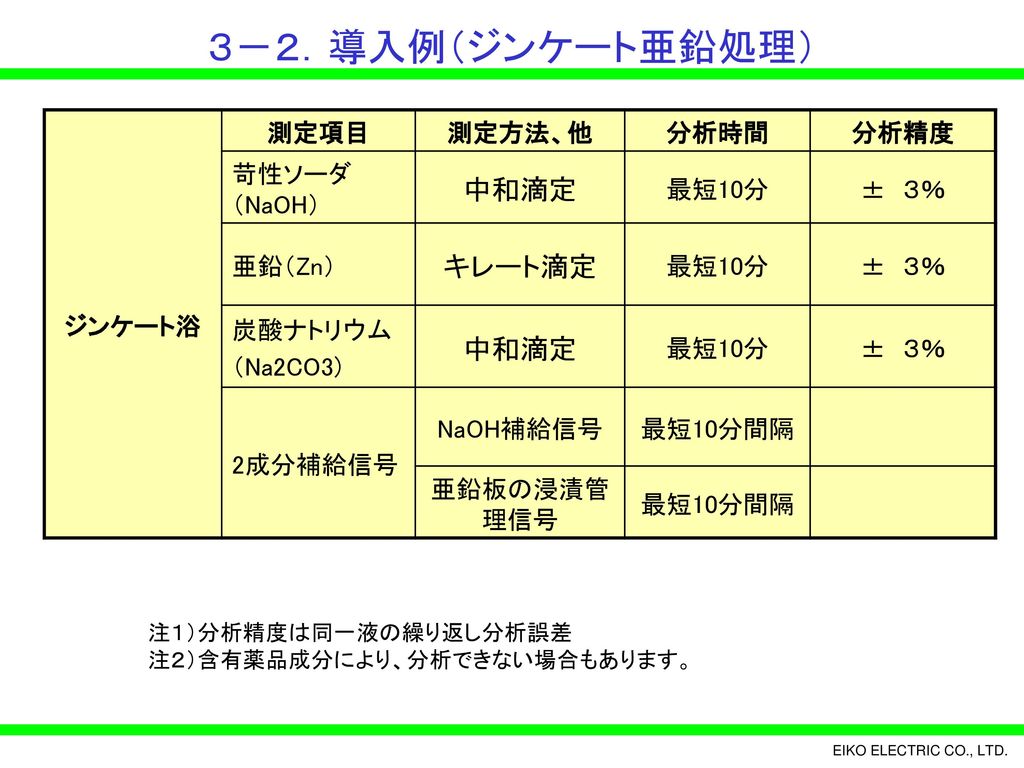



Blogjpmbahetwfl 無料ダウンロード キレート滴定 計算 亜鉛 キレート滴定 計算 亜鉛
滴定の終点における水溶液の色の変化を化学式で説明して下さい. ④ MXについて調べてみましょう。 ⑤ 「1モル塩化アンモニウム添加」の理由を、化学平衡の移動原理で説明してみましょう。 ⑥ テキストp137の参考の2.について考察してみましょう。44 キレート滴定の条件とph 45 edtaおよびntaによるキレート滴定の条件 46 金属指示薬とは何か 47 キレート滴定の種類 48 錯生成反応を支配する因子 演習問題 問題解答 5.酸化還元反応と酸化還元滴定 51 電極電位とネルンスト式の理解 · キレート滴定法のほか、icp 発光分光分析法も硬度の測定方法の一つです。icp 発光分光分析法は、プラズマ に導き入れた試料中のカルシウム等が発する光を測定して、その濃度を求める方法です。ではプラズマとは何で しょうか。




Pdf Ecotoxicological Assessment Of Industrial Effluents Toxicity Characterization And Impact On Receiving Water




The Chemioal Chemical Society Sooiety Of Japan 生成反応がすすむため 沈殿は Cu Nh3 4p を作り つつ溶解する このため濃度の大きい場合ほど その頂 とが確認でき 錯体化学における当量関係を理解させ 一助とすることができた 点勾 Pdf Free Download
キレート滴定 多座配位子EDTA(標準液)が 金属イオン(Zn 2, Mg 2, Ca , Al3, Cu 等)と 水溶液中で安定な可溶性のキレート化合物を生成する ことを利用した滴定法 →容量分析による金属イオンの定量法 *滴定終点判定法は次週に解説する 9 キレート滴定のキレート滴定 エチレンジアミン四酢酸(edta、h 4 yと略記)は、水溶液中で金属イオンと反応し、 非常に安定な金属キレート化合物を作る。 キレート滴定は、そのことを利用した容量分析法である。キレート生成反応は、 である。 · そこで、滴定の終点を見えるようにするため、 EBT(エリオクロムブラックT) などの指示薬を使用します。 EBTを指示薬とした場合、 赤 → 青 となった時点を終点とできます EBTもキレート剤として働き、Ca、Mgなどと錯体を形成した際、赤色を示します。 しかし、金属イオンから離れると青色を示すという性質を利用してEDTA法の指示薬となります。 まず




Mbaheblogjpxy1z 無料でダウンロード キレート滴定 Ph キレート滴定 Ph 理由
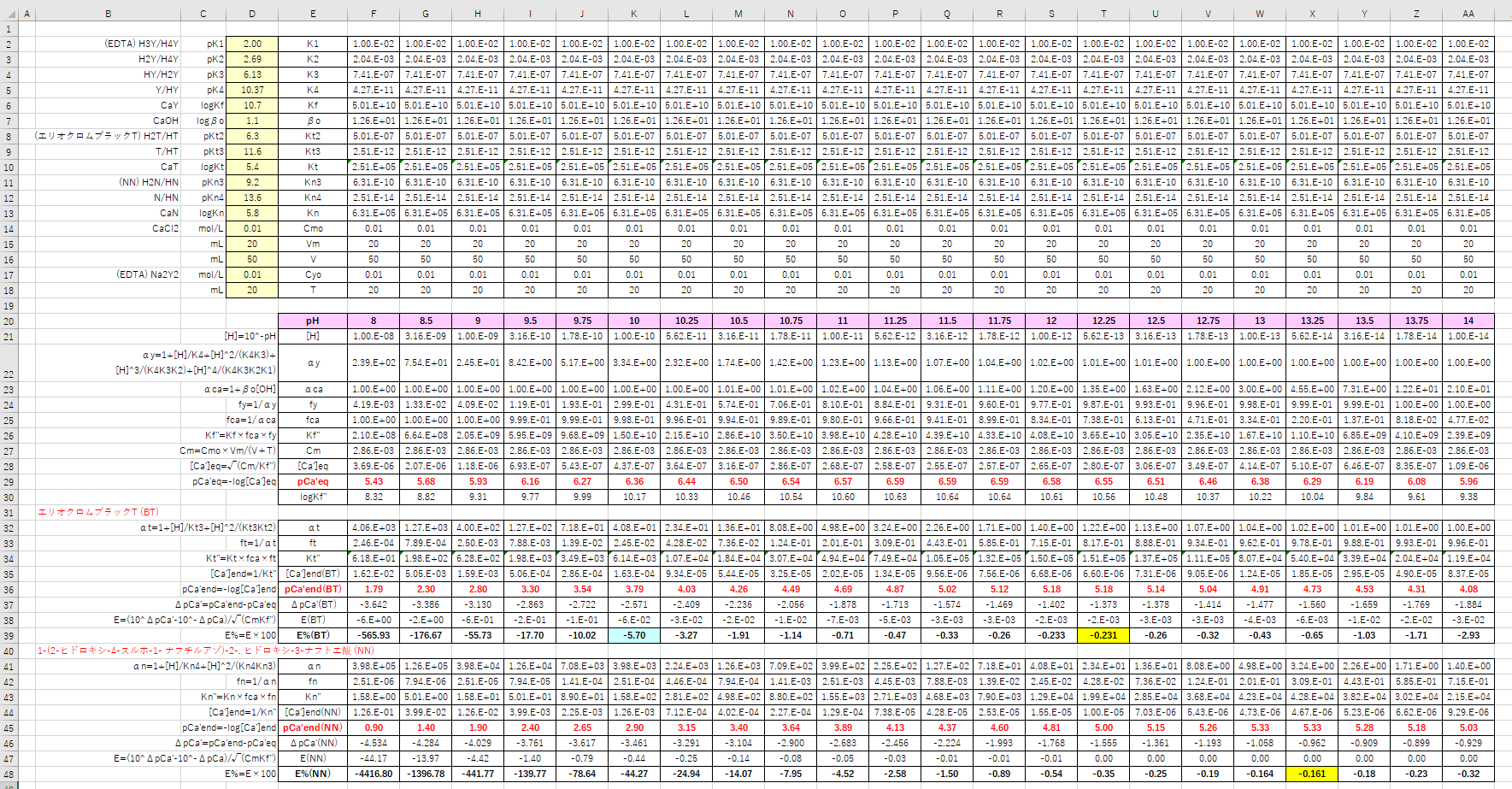



滴定 滴定曲線 溶解度などーエクセルを用いて
となる。 キレート滴定では、この至適 pH を保つために緩衝液が用いられる! XIII13 補助錯化剤 一般にキレート滴定はかなり高い pH で行なうが、このとき金属水酸化物を沈殿させな いように、 EDTA より Kf の小さい錯化剤(=補助錯化剤 )を共存させることがある · 実験レポートでもっとも苦労するのが「考察」です. ここは得られた結果から何が言えるのか,「あなたの考えを述べるところです」. なんですが, そもそも考察って,何でしょうか? · )250枚 急ぎでお願いします 化学で水の硬度測定でキレート滴定をしました その考察で ベストアンサー:吸収波長が変われば色が変わる。 光の波長が違えば色も違うから。




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog
法法法法という。EDTAは水にほとんど溶けないので、キレート滴定では水に溶けやすいEDTA ・2Naを用いる。 全硬度の測定は、試料水のpHを約10 に調整した後,BT指示薬を加えて、EDTA溶洷 で滴定して求める。101 青井 仁美 飲むヨーグルト中のカルシウム濃度の測定と比較 1 秋田 萌 102 飯村 祥子 飲料水のキレート滴定 2 石垣 裕美 市販の清涼飲料水中のカルシウム濃度 103 石橋 久美子 様々な飲料の酸濃度の滴定 3 井上 紘子 様々な飲料の酸(キレート滴定編) 181 日本工業化学教育研究会 高校生ものづくりコンテスト化学分析部門研究委員会 読み取り、滴定後の使用量を求める(jis k 0050 附属書 c



キレート滴定法のマイクロスケール化



キレート滴定法のマイクロスケール化
· キレート滴定の実験で 色の変化が起こる原因を考察しなさい ってゆー項目があるんですけど、お願い ベストアンサー:一つの具体例: EBT(H3In) を金属変色指示薬として、pH=8~10 程度に維持し EDTA(H4Y) で金属イオン「M^2」をキレート滴定する場合の、当量点キレート滴定きれーとてきていchelatometric titration 金属イオン が多座 配位子 で囲まれて安定な錯化合物を生成するとき、その化合物を キレート というが、多くの金属イオンと安定なキレートを生成する EDTA ( エチレンジアミン四酢酸 )およびその類縁EDTA(エチレンジアミン四酢酸)は、最大6本の腕(6座配位)で2価~4価の金属イオンと、そのイオンの価数に関係なく1:1で結合し、安定なキレート化合物を生成する。 この反応を利用した金属イオンの定量法をキレート滴定法という。 (キレートとはカニのはさみの意味) なお、EDTAは水にほとんど溶けないため、キレート滴定では水に溶けやすいEDTA・2Naを用いる




Images Of 中和滴定 Japaneseclass Jp
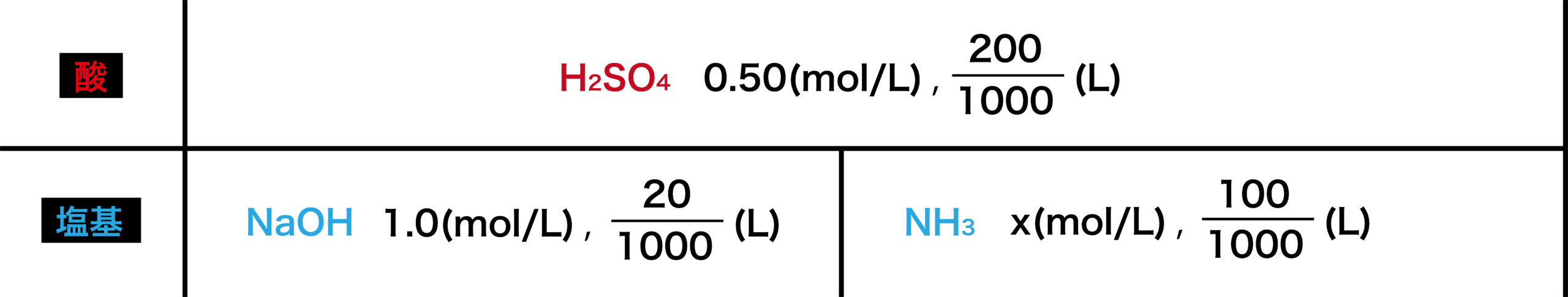



逆滴定 例題 計算問題の解き方 原理など 化学のグルメ
キレート滴定法は比較的短時間にかつ簡便な操作で行 うことができ,測定精度に優れているなど,金 属標準液 の標定には有利な特性を備えているバ リウムの直接滴 定法としてはο一クレゾールフタレイン
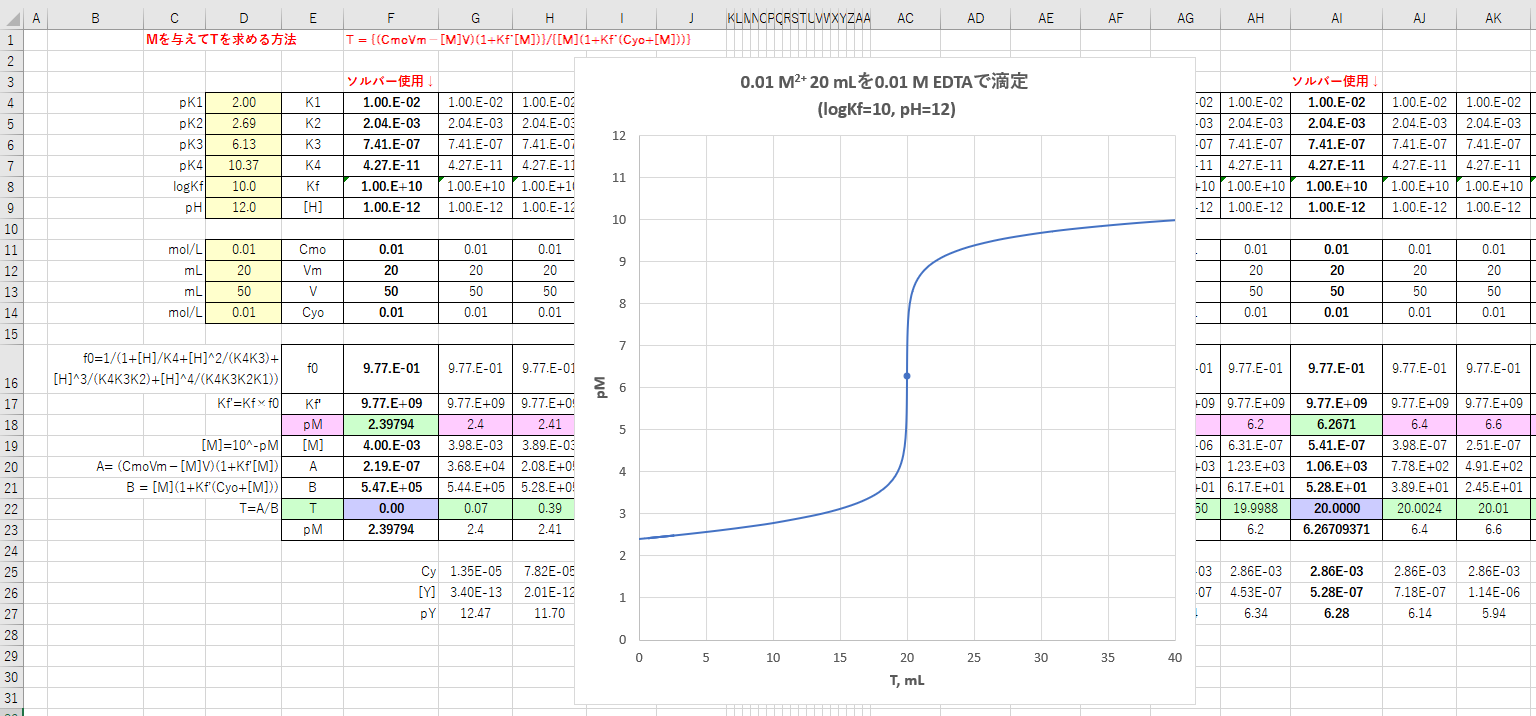



Edta滴定の基礎 滴定曲線 溶解度などーエクセルを用いて
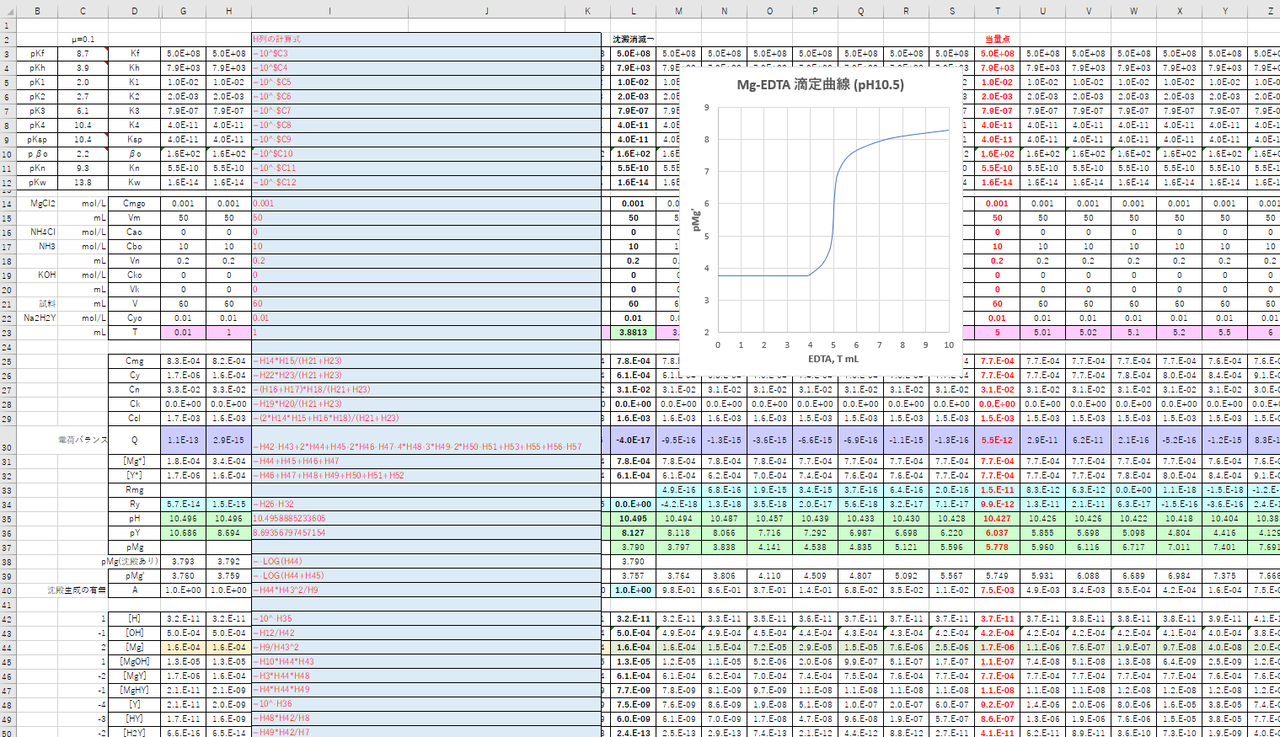



年05月 滴定曲線 溶解度などーエクセルを用いて




滴定法の入門 臨床検査 4巻3号 医書 Jp



0 件のコメント:
コメントを投稿